A Titulação Ácido-Base é uma técnica laboratorial quantitativa fundamental usada para determinar a concentração desconhecida de um ácido ou base dissolvido. Ao reagir uma solução de concentração desconhecida com uma solução de concentração precisamente conhecida (o titulante), os cientistas podem usar a estequiometria da reação química para calcular a molaridade exata da amostra. Este é o método principal usado para tudo, desde testar a acidez do vinho até garantir a potência de antiácidos líquidos.
Como Funciona a Titulação Ácido-Base
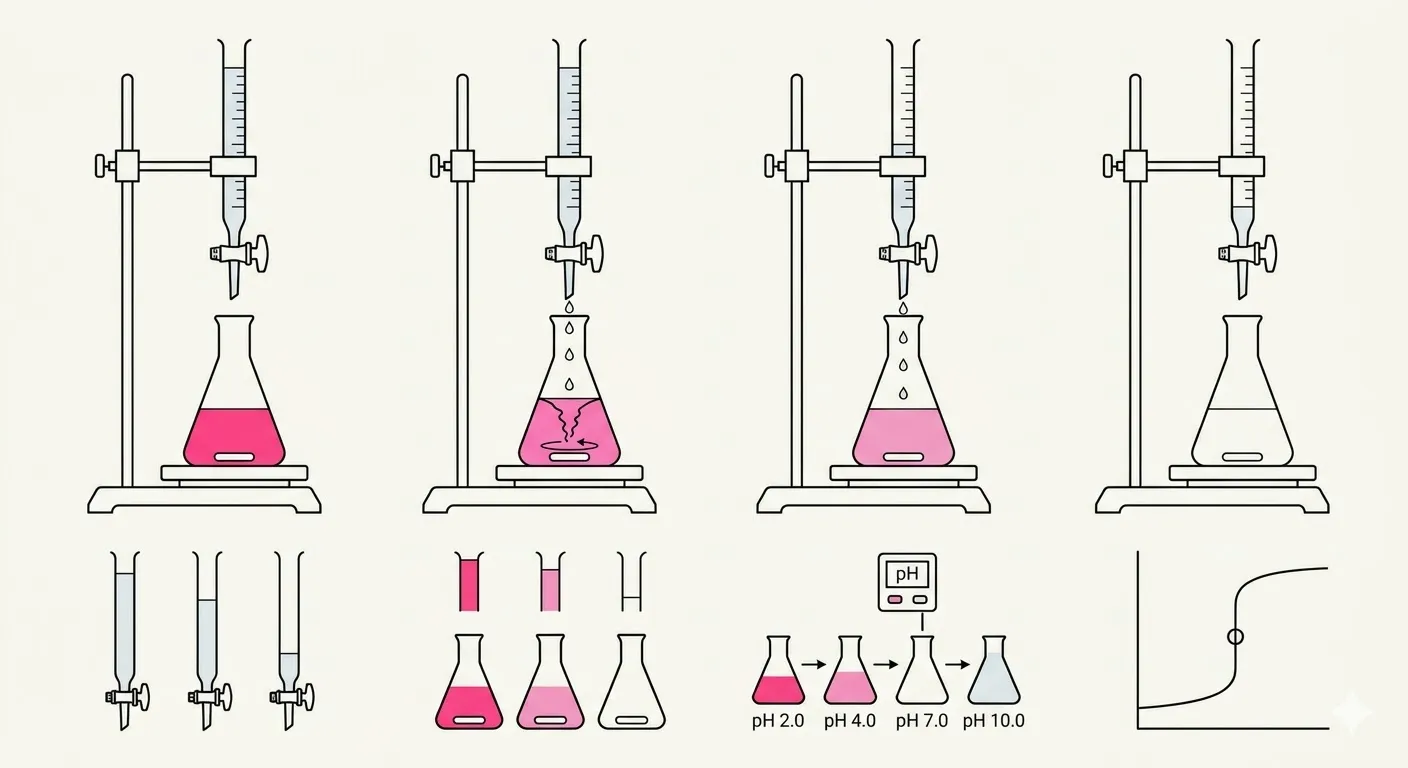
O processo depende de uma “batalha” química controlada onde o ponto de vitória é alcançado quando o ácido e a base se neutralizaram perfeitamente.
Um volume preciso da solução desconhecida, chamada de analito, é colocado em um erlenmeyer com algumas gotas de um indicador de pH como fenolftaleína, enquanto uma bureta é preenchida com o titulante de concentração conhecida. A torneira da bureta é aberta para permitir que o titulante flua para o frasco, onde ocorre uma reação de neutralização — por exemplo, a titulação de ácido clorídrico com hidróxido de sódio produz água e sal: HCl + NaOH → H2O + NaCl. O objetivo é atingir o ponto de equivalência, onde o número de mols de titulante adicionado é quimicamente igual ao número de mols da substância na amostra desconhecida, significando que o ácido e a base se neutralizaram completamente. Como o ponto de equivalência é invisível, o ponto final é usado em seu lugar — o momento em que o indicador de pH muda de cor permanentemente, como passar de incolor para um rosa persistente muito tênue, sinalizando ao cientista para interromper o fluxo imediatamente. Medindo exatamente quantos mililitros de titulante foram usados da bureta e conhecendo a molaridade do titulante, a concentração do desconhecido pode ser calculada usando a fórmula Macid × Vacid = Mbase × Vbase (assumindo uma proporção molar de 1:1; coeficientes são adicionados para outras proporções).
recurso: Ferramenta de titulação ácido-base do Lab Lexicon
