酸碱滴定是一种基本的定量实验室技术,用于测定溶解的酸或碱的未知浓度。通过将未知浓度的溶液与浓度精确已知的溶液(滴定剂)进行反应,科学家可以利用化学反应的化学计量关系来计算样品的精确摩尔浓度。这是从测试葡萄酒的酸度到确保液体抗酸剂效力等各种应用的主要方法。
酸碱滴定原理
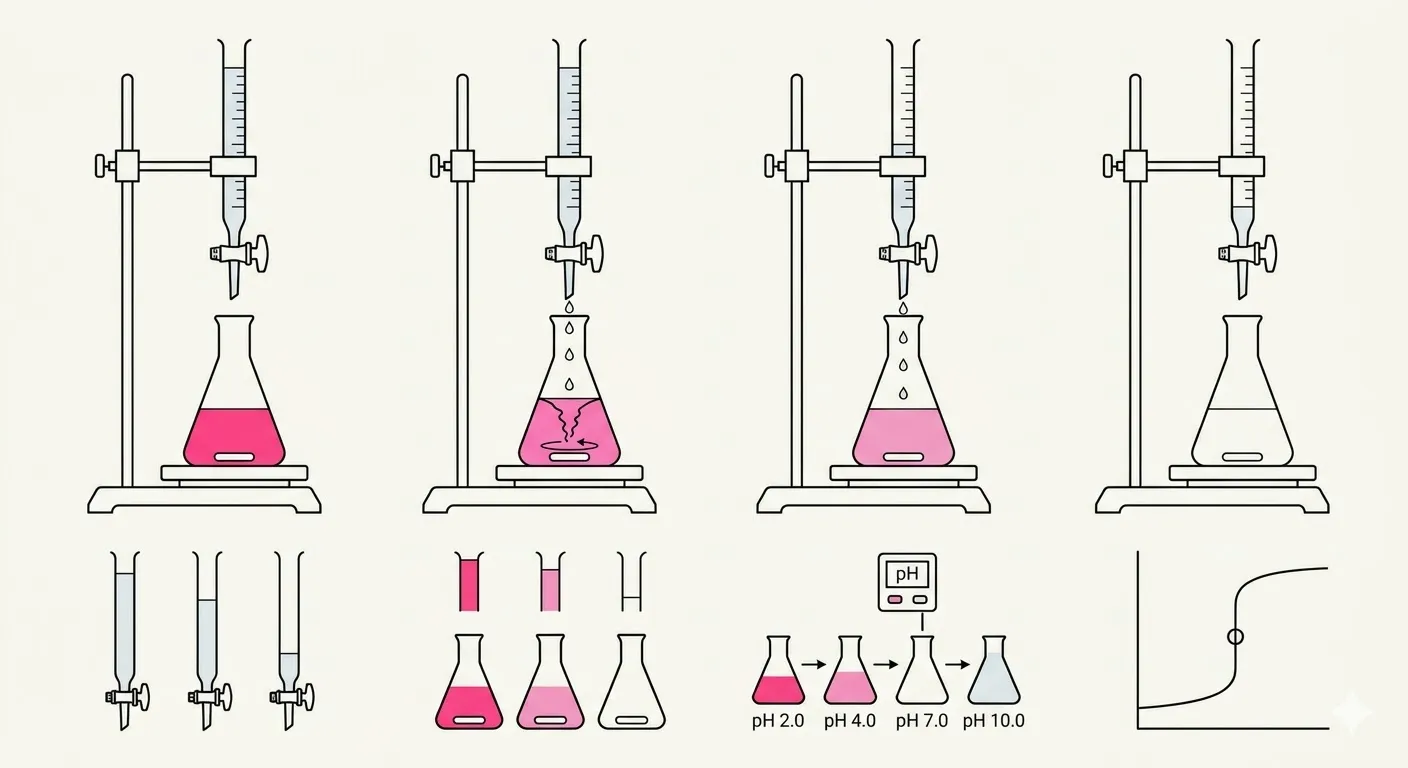
该过程依赖于可控的化学”对抗”,当酸和碱完全中和时即达到终点。
将精确体积的未知溶液(待测物)置于锥形瓶中,加入几滴 pH 指示剂(如酚酞),同时用已知浓度的滴定剂装满滴定管。打开滴定管的活塞,让滴定剂流入烧瓶,发生中和反应——例如,用盐酸滴定氢氧化钠生成水和盐:HCl + NaOH → H2O + NaCl。目标是达到当量点,此时加入的滴定剂的摩尔数在化学上等于未知样品中物质的摩尔数,意味着酸和碱已完全中和。由于当量点不可见,使用终点代替——即 pH 指示剂发生永久性颜色变化的时刻,例如从透明变为非常淡且持久的粉红色,提示科学家立即停止滴定。通过精确测量滴定管中使用的滴定剂毫升数并已知滴定剂的摩尔浓度,可以使用公式 Macid × Vacid = Mbase × Vbase 计算未知物的浓度(假设摩尔比为 1:1;其他比例需添加系数)。
资源: 实验室酸碱滴定工具
