Die Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese (SDS-PAGE) ist eine leistungsstarke Labortechnik, mit der Proteine ausschließlich anhand ihres Molekulargewichts getrennt werden. Wissenschaftler beschäftigen sich häufig mit „Proteinsuppen“ – komplexen Mischungen, die Hunderte verschiedener Arten von Proteinen enthalten. SDS-PAGE fungiert als Molekularsieb und ermöglicht es Forschern, diese Mischung zu entwirren, um bestimmte Proteine zu identifizieren, die Reinheit einer Probe zu überprüfen oder die Größe eines synthetisierten Proteins zu überprüfen.
So funktioniert SDS-PAGE
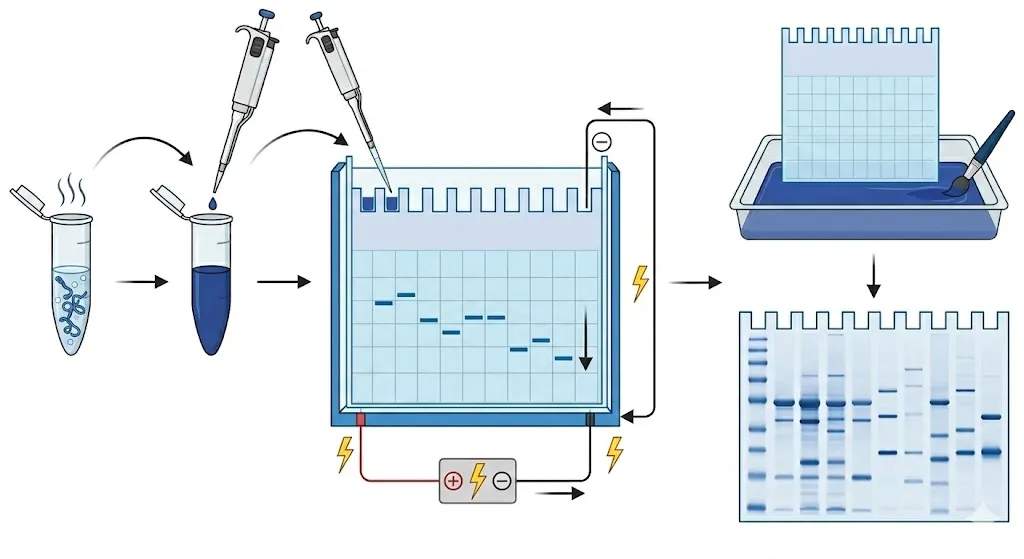
Der Prozess beruht auf der Tatsache, dass Proteine im Gegensatz zur DNA komplexe, gefaltete Formen und unterschiedliche natürliche Ladungen haben. Um sicherzustellen, dass die Größe der einzige Faktor ist, der ihre Bewegung beeinflusst, verwendet das Experiment eine Reihe von Schritten, um die Proteineigenschaften „zurückzusetzen“.
- Denaturierung
Die Proteinprobe wird mit einem Puffer, der SDS (ein starkes Detergens) enthält, gemischt und erhitzt. Das SDS fungiert als chemischer Glättapparat; Es entfaltet die komplexe 3D-Struktur der Proteine in lineare Ketten. Entscheidend ist, dass das SDS die Proteine mit einer gleichmäßigen negativen Ladung umhüllt und so sicherstellt, dass sie sich unabhängig von ihrer ursprünglichen Ladung zur positiven Elektrode bewegen.
- Laden
Die Probe wird in die Vertiefungen eines Polyacrylamidgels geladen – einer synthetischen Matrix, die als mikroskopischer Hindernisparcours fungiert. Eine „Proteinleiter“ (eine Mischung aus Proteinen mit bekannten Molekulargewichten) wird typischerweise in die erste Vertiefung geladen, um als Maßstab für den Rest des Experiments zu dienen.
- Migration
An das Gel wird ein elektrischer Strom angelegt. Da die Proteine negativ geladen sind, bewegen sie sich in Richtung der Anode (positive Elektrode) unten. Auf ihrer Reise navigieren kleinere Proteine mühelos und schnell durch die Poren des Gels, während größere Proteine sich verheddern und sich viel langsamer bewegen.
- Visualisierung
Nach Abschluss der Elektrophorese sind die Proteine für das bloße Auge unsichtbar. Das Gel ist mit einem Fleck getränkt – am häufigsten Coomassie Brilliant Blue. Der Farbstoff bindet an die Proteine und zeigt eine Reihe deutlicher blauer Banden. Durch den Vergleich der Position dieser Banden mit der Proteinleiter können Wissenschaftler das genaue Molekulargewicht jedes Proteins in der Probe berechnen.
