L’électrophorèse sur gel de polyacrylamide en présence de dodécylsulfate de sodium (SDS-PAGE) est une puissante technique de laboratoire utilisée pour séparer les protéines exclusivement en fonction de leur poids moléculaire. Les scientifiques sont souvent confrontés à des « soupes de protéines » — des mélanges complexes contenant des centaines de types de protéines différents. Le SDS-PAGE agit comme un tamis moléculaire, permettant aux chercheurs de démêler ce mélange pour identifier des protéines spécifiques, vérifier la pureté d’un échantillon ou confirmer la taille d’une protéine synthétisée.
Comment Fonctionne le SDS-PAGE
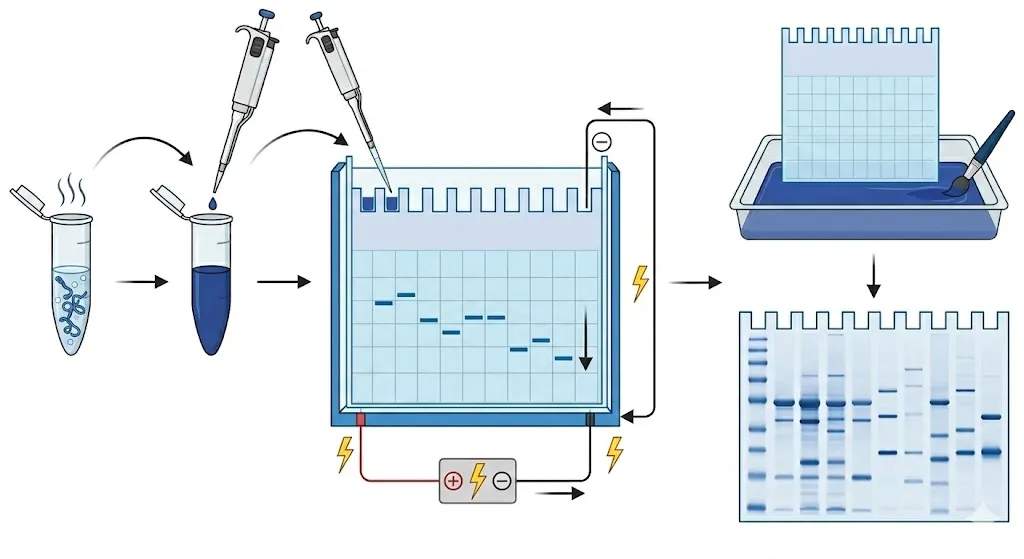
Le processus repose sur le fait que les protéines, contrairement à l’ADN, ont des formes repliées complexes et des charges naturelles variables. Pour garantir que la taille soit le seul facteur influençant leur déplacement, l’expérience utilise une série d’étapes pour « réinitialiser » les propriétés des protéines.
- Dénaturation
L’échantillon de protéines est mélangé avec un tampon contenant du SDS (un détergent puissant) et chauffé. Le SDS agit comme un défrisant chimique ; il déplie la structure 3D complexe des protéines en chaînes linéaires. Crucialement, le SDS enrobe les protéines d’une charge négative uniforme, garantissant qu’elles se déplacent vers l’électrode positive quelle que soit leur charge d’origine.
- Chargement
L’échantillon est déposé dans les puits d’un gel de polyacrylamide — une matrice synthétique qui agit comme un parcours d’obstacles microscopique. Un « marqueur de poids moléculaire » (un mélange de protéines de poids moléculaires connus) est généralement chargé dans le premier puits pour servir de règle pour le reste de l’expérience.
- Migration
Un courant électrique est appliqué à travers le gel. Parce que les protéines sont chargées négativement, elles se déplacent vers l’anode (électrode positive) en bas. En voyageant, les petites protéines naviguent facilement à travers les pores du gel et se déplacent rapidement, tandis que les plus grosses protéines s’emmêlent et se déplacent beaucoup plus lentement.
- Visualisation
Après la fin de l’électrophorèse, les protéines sont invisibles à l’œil nu. Le gel est trempé dans un colorant — le plus souvent le bleu de Coomassie Brillant. Le colorant se lie aux protéines, révélant une série de bandes bleues distinctes. En comparant la position de ces bandes au marqueur de poids moléculaire, les scientifiques peuvent calculer le poids moléculaire exact de chaque protéine dans l’échantillon.
