Le Titrage Acido-Basique est une technique quantitative fondamentale de laboratoire utilisée pour déterminer la concentration inconnue d’un acide ou d’une base dissous. En faisant réagir une solution de concentration inconnue avec une solution de concentration précisément connue (le titrant), les scientifiques peuvent utiliser la stœchiométrie de la réaction chimique pour calculer la molarité exacte de l’échantillon. C’est la méthode principale utilisée pour tout, du test de l’acidité du vin à la vérification de l’efficacité des antiacides liquides.
Comment Fonctionne le Titrage Acido-Basique
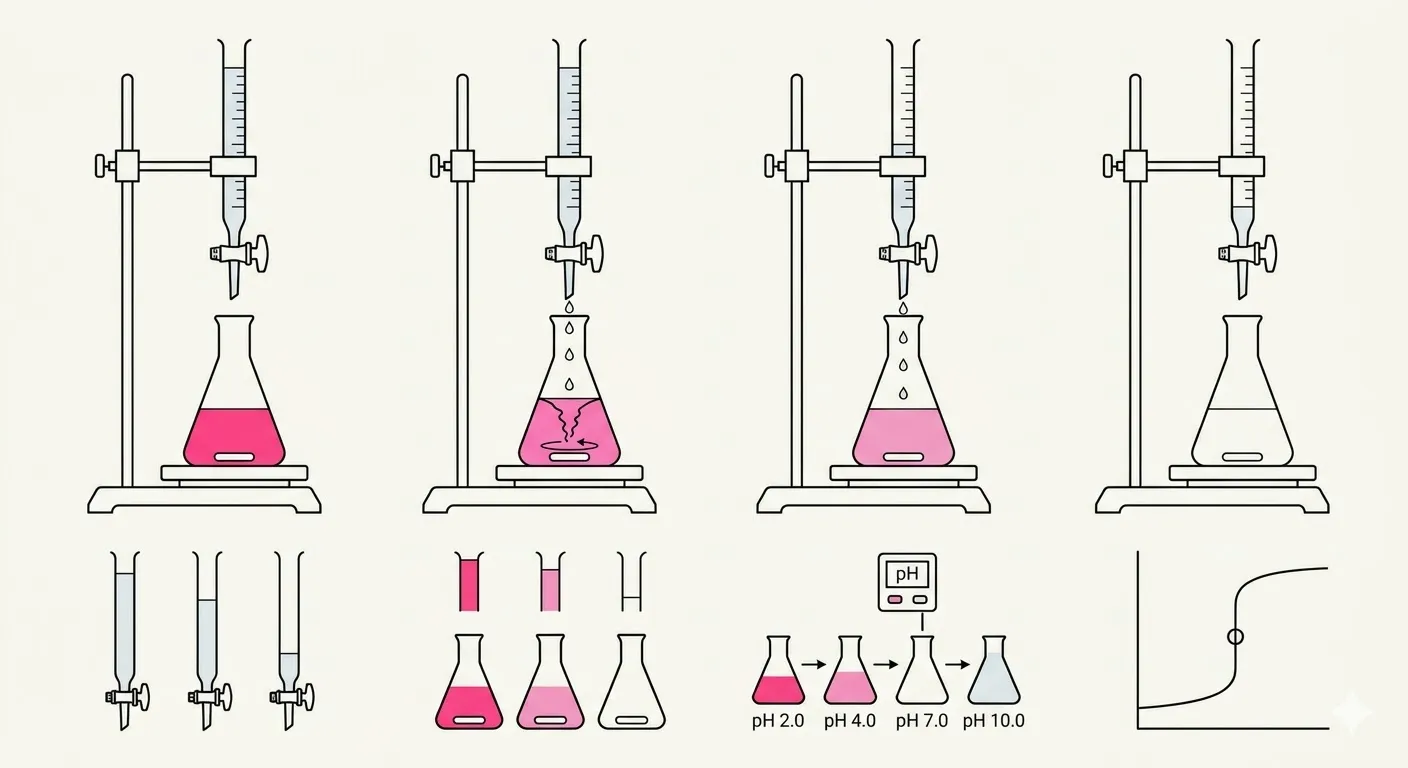
Le processus repose sur une “bataille” chimique contrôlée où le point de victoire est atteint lorsque l’acide et la base se sont parfaitement neutralisés.
Un volume précis de la solution inconnue, appelée l’analyte, est placé dans un erlenmeyer avec quelques gouttes d’un indicateur de pH tel que la phénolphtaléine, tandis qu’une burette est remplie du titrant de concentration connue. Le robinet de la burette est ouvert pour permettre au titrant de s’écouler dans le flacon, où une réaction de neutralisation se produit — par exemple, le titrage de l’acide chlorhydrique avec l’hydroxyde de sodium produit de l’eau et du sel : HCl + NaOH → H2O + NaCl. Le but est d’atteindre le point d’équivalence, où le nombre de moles de titrant ajouté est chimiquement égal au nombre de moles de la substance dans l’échantillon inconnu, ce qui signifie que l’acide et la base se sont complètement neutralisés. Comme le point d’équivalence est invisible, le point final est utilisé à la place — le moment où l’indicateur de pH change de couleur de façon permanente, par exemple passant d’incolore à un rose très pâle persistant, signalant au scientifique d’arrêter immédiatement le flux. En mesurant exactement combien de millilitres de titrant ont été utilisés depuis la burette et en connaissant la molarité du titrant, la concentration de l’inconnu peut être calculée en utilisant la formule Macide × Vacide = Mbase × Vbase (en supposant un rapport molaire 1:1 ; des coefficients sont ajoutés pour d’autres rapports).
ressource : Outil de titrage acido-basique Lab Lexicon
