Titrasi Asam-Basa adalah teknik laboratorium kuantitatif fundamental yang digunakan untuk menentukan konsentrasi asam atau basa terlarut yang tidak diketahui. Dengan mereaksikan larutan dengan konsentrasi yang tidak diketahui dengan larutan dengan konsentrasi yang diketahui secara presisi (titran), ilmuwan dapat menggunakan stoikiometri reaksi kimia untuk menghitung molaritas sampel secara tepat. Ini adalah metode utama yang digunakan untuk segala hal mulai dari menguji keasaman anggur hingga memastikan potensi antasida cair.
Bagaimana Titrasi Asam-Basa Bekerja
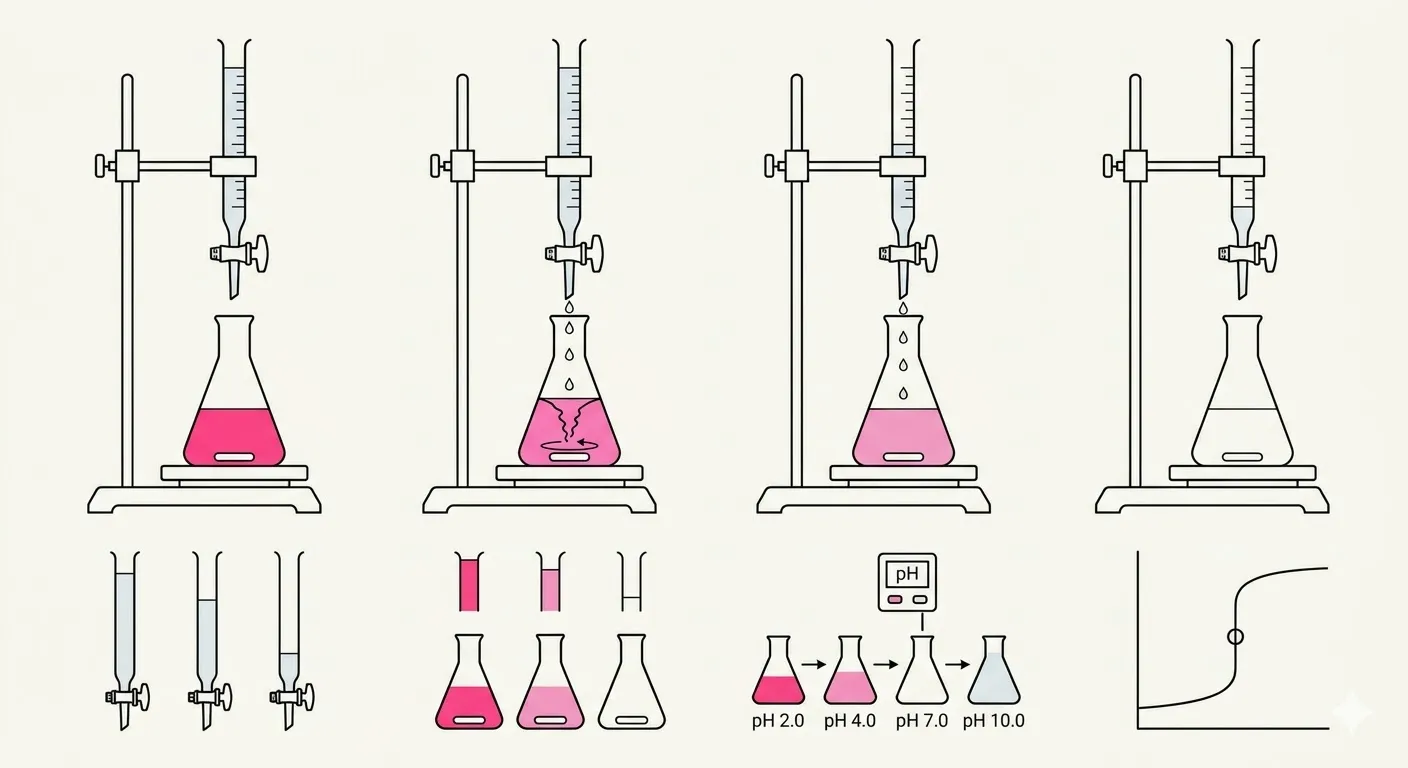
Proses ini bergantung pada pertarungan kimia yang terkontrol di mana titik kemenangan tercapai ketika asam dan basa telah saling menetralkan dengan sempurna.
Volume presisi dari larutan yang tidak diketahui, yang disebut analit, ditempatkan dalam labu Erlenmeyer dengan beberapa tetes indikator pH seperti fenolftalein, sementara buret diisi dengan titran dengan konsentrasi yang diketahui. Keran buret dibuka untuk memungkinkan titran mengalir ke dalam labu, di mana reaksi netralisasi terjadi — misalnya, mentitrasi asam klorida dengan natrium hidroksida menghasilkan air dan garam: HCl + NaOH → H2O + NaCl. Tujuannya adalah mencapai titik ekuivalen, di mana jumlah mol titran yang ditambahkan secara kimia sama dengan jumlah mol zat dalam sampel yang tidak diketahui, artinya asam dan basa telah sepenuhnya menetralkan satu sama lain. Karena titik ekuivalen tidak terlihat, titik akhir digunakan sebagai gantinya — saat indikator pH berubah warna secara permanen, seperti berubah dari bening menjadi merah muda sangat pucat yang persisten, menandakan ilmuwan untuk menghentikan aliran segera. Dengan mengukur secara tepat berapa mililiter titran yang digunakan dari buret dan mengetahui molaritas titran, konsentrasi yang tidak diketahui dapat dihitung menggunakan rumus Masam × Vasam = Mbasa × Vbasa (dengan asumsi rasio mol 1:1; koefisien ditambahkan untuk rasio lainnya).
resource: Alat titrasi asam/basa Lab Lexicon
